9급 지방직 공무원 화학(2017. 12. 16.) 시험일자 : 2017년 12월 16일
1. 계의 엔트로피가 증가하는 과정은?
- ① Ag+(aq)+Cl-(aq)→AgCl(s)
- ② 4Fe(s)+3O2(g)→2Fe2O3(s)
- ③ HCl(g)+NH3(g)→NH4Cl(s)
- ④ 2SO3(g)→2SO2(g)+O2(g)
등록된 댓글이 없습니다.
2. CN-이온의 루이스 구조에서 N의 형식 전하는?
- ① 0
- ② +1
- ③ +2
- ④ +3
등록된 댓글이 없습니다.
3. 그림에서 설명하는 분자간 힘은?
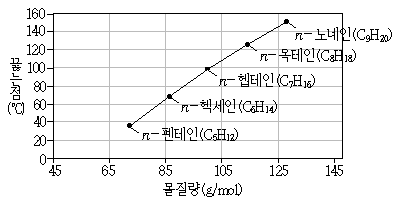
- ① 쌍극자-쌍극자 힘
- ② 이온-쌍극자 힘
- ③ 수소 결합
- ④ 분산력
등록된 댓글이 없습니다.
4. 다음 중 화학 결합의 종류가 다른 것은?
- ① 염화 소듐(NaCl)
- ② 물(H2O)
- ③ 일염화 아이오딘(ICl)
- ④ 암모니아(NH3)
등록된 댓글이 없습니다.
5. 다음 화합물의 수용액이 산성인 것만을 모두 고른 것은?
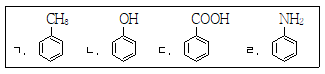
- ① ㄱ, ㄷ
- ② ㄴ, ㄷ
- ③ ㄴ, ㄹ
- ④ ㄷ, ㄹ
등록된 댓글이 없습니다.
6. 원자가 껍질 전자쌍 반발(VSEPR) 이론에 의한 ClO3+이온의 기하학적 구조는?
- ① 굽은형
- ② 정사면체
- ③ 삼각 평면
- ④ 평면 사각형
등록된 댓글이 없습니다.
7. 일양성자 산 1.0M HA용액의 H+농도[M]는? (단, 약산 HA의 산 해리 상수 Kα=4.0×10-1이다)
- ① 2.0×10-5
- ② 4.0×10-5
- ③ 2.0×10-10
- ④ 4.0×10-10
ㅇㅇ2022. 6. 21. 02:11삭제
10승인 거 같은데 1로 된 듯
8. 다음 전자 배치에 해당하는 원자들에 대한 설명으로 옳은 것만을 모두 고른 것은?

- ① ㄱ, ㄴ
- ② ㄱ, ㄷ
- ③ ㄴ, ㄷ
- ④ ㄱ, ㄴ, ㄷ
등록된 댓글이 없습니다.
9. 다음 반응식에서 각 반응물의 농도를 달리하며 초기 반응 속도를 측정하여 아래 표와 같은 결과를 얻었다. (단, 반응 온도는 일정하다) 위 반응의 속도 법칙은?
- ① k[ClO2][OH-]
- ② k[ClO2]2[OH-]
- ③ k[ClO2][OH-]2
- ④ k[ClO2]2[OH-]2
등록된 댓글이 없습니다.
10. 이산화 탄소(CO2)가 127℃에서 300m/s의 평균 속력으로 움직인다면 1327℃에서의 CO2의 평균 속력[m/s]은? (단, CO2는 두 온도에서 이상 기체의 거동을 보인다고 가정한다)
- ① 1200
- ② 900
- ③ 600
- ④ 300
등록된 댓글이 없습니다.
11. 다음 산-염기 반응에 대한 설명으로 옳은 것은?
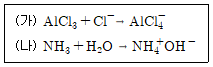
- ① (가)에서 AlCl3는 아레니우스 산이다.
- ② (가)에서 Cl-는 루이스 산이다.
- ③ (나)에서 NH3는 루이스 산이다.
- ④ (나)에서 H2O는 브뢴스테드-로우리 산이다.
등록된 댓글이 없습니다.
12. 질소 산화물에 대한 설명으로 옳은 것만을 모두 고른 것은?

- ① ㄱ, ㄷ
- ② ㄱ, ㄹ
- ③ ㄴ, ㄷ
- ④ ㄴ, ㄹ
등록된 댓글이 없습니다.
13. 수산화 소듐(NaOH) 4g을 물에 녹여 200mL의 수산화 소듐 수용액을 만들었다. 이 수용액 20mL를 0.25M HCl로 중화하는데 필요한 HCl의 부피[mL]는? (단, NaOH의 몰질량은 40g/mol이다)
- ① 20
- ② 40
- ③ 60
- ④ 80
등록된 댓글이 없습니다.
14. 커피에서 카페인을 초임계 추출할 때 용매로 사용되는 이산화 탄소의 상을 다음 상도표에서 고르면?
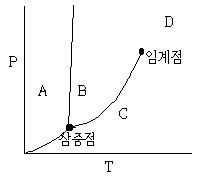
- ① A
- ② B
- ③ C
- ④ D
등록된 댓글이 없습니다.
15. 그림과 같이 아연(Zn)판을 황산구리(CuSO4) 수용액에 넣었을 때 일어나는 반응에 대한 설명으로 옳은 것만을 모두 고른 것은?
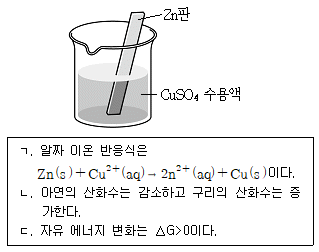
- ① ㄱ
- ② ㄷ
- ③ ㄱ, ㄴ
- ④ ㄴ, ㄷ
등록된 댓글이 없습니다.
16. 산화-환원 반응이 아닌 것은?
- ① 2Mg(s)+O2(g)→2MgO(s)
- ② 4KNO3(s)→2K2O(s)+2N2(g)+5O2(g)
- ③ NaHSO4(aq)+NaOH(aq)→Na2SO4(aq)+H2O(l)
- ④ Fe(s)+Ni(NO3)2(aq)→Fe(NO3)2(aq)+Ni(s)
등록된 댓글이 없습니다.
17. 일정한 온도에서 1atm의 H2 2L, 2atm의 O2 3L, 3atm의 N2 4L를 10L의 밀폐된 용기에 넣었을 때의 전체 압력[atm]은? (단, 세 기체는 서로 반응하지 않는 이상 기체라고 가정한다)
- ① 1
- ② 2
- ③ 3
- ④ 4
등록된 댓글이 없습니다.
18. 아래 그림은 반응 경로에 따른 에너지 변화를 나타낸 것이다. 이 때 옳은 것만을 모두 고른 것은?
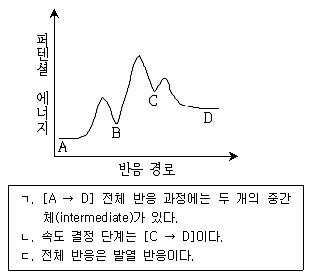
- ① ㄱ
- ② ㄷ
- ③ ㄱ, ㄴ
- ④ ㄴ, ㄷ
등록된 댓글이 없습니다.
19. 바닥 상태인 2주기 원소 X, Y의 홀전자(unpaired electron) 수는 같고, 값이 X=1, Y=2/3이다. 이에 대한 설명으로 옳은 것은?
- ① 원자가 전자(valence electron)수는 X가 Y보다 많다.
- ② 유효 핵전하는 X가 Y보다 크다.
- ③ 원소 Y가 수소(H)와 결합한 화합물은 YH3이다.
- ④ 화합물 XY2는 직선형이다.
등록된 댓글이 없습니다.
20. 다음 반응식의 균형을 맞추었을 때, H2O의 계수는?
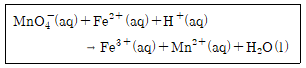
- ① 2
- ② 3
- ③ 4
- ④ 6
등록된 댓글이 없습니다.